
Węglowodory aromatyczne mają strukturę cykliczną. Pierwszym przedstawicielem tej serii jest benzen (C6H6). Formuła odzwierciedlająca strukturę materii została po raz pierwszy zaproponowana przez chemika Kekule w 1865 roku. Według naukowca przez długi czas zastanawiał się nad zagadką benzenu. Pewnej nocy śnił o wężu gryzącym jego ogon. Rano opracowano już wzór strukturalny benzenu. Był to pierścień składający się z 6 atomów węgla. Trzy z nich miały podwójne połączenie.

Węgiel w kompozycji aromatycznych węglowodorówtworzy regularny sześciokąt. Czasami, pisząc równania reakcji, jest on wyciągany w kierunku pionowym. Ta grupa atomów otrzymała specjalną nazwę - jądro benzenu. Potwierdzeniem cyklicznej struktury benzenu jest jego produkcja z trzech cząsteczek acetylenu - nienasyconego węglowodoru z potrójnym wiązaniem. Węglowodory aromatyczne są również nienasycone i wykazują pewne właściwości charakterystyczne dla alkenów. Z tego powodu w pierścieniu benzenowym trzy kreski biegnące równolegle do powierzchni wskazują podwójne wiązanie. Ta formuła benzenu nie odzwierciedla w pełni stanu atomów węgla w cząsteczce.

W rzeczywistości więź między węglem w pierścieniusą sobie równe. Wśród nich nie można było wyróżnić pojedynczego ani podwójnego. Ta cecha jest wyjaśniona przez strukturę elektronową benzenu, w której węgiel w jądrze znajduje się w sp2-hybrydyzowany stan, podłączony do sąsiadówna pierścieniu i wodorze za pomocą trzech zwykłych pojedynczych wiązań. W tym przypadku pojawia się sześciokąt, w którym 6 atomów węgla i 6 atomów wodoru znajduje się w jednej płaszczyźnie. Tylko chmury elektronowe czwartych elektronów p nie biorących udziału w hybrydyzacji są ułożone inaczej. Ich kształt przypomina hantle, środek znajduje się na płaszczyźnie pierścienia. A pogrubione części są na górze i na dole. W tym przypadku, powyżej jądra benzenowego i poniżej niego, występują dwie gęstości elektronowe, które pojawiły się podczas zachodzenia na siebie chmur elektronowych p-elektronów. W pierścieniu występuje ogólne wiązanie chemiczne węgla.
Ze względu na całkowitą gęstość elektronów,odległość między węglem w pierścieniu. Są równe 0,14 nm. Gdyby istniały pojedyncze i podwójne wiązania w rdzeniu benzenowym, pojawiłyby się dwa wskaźniki: 0,134 i 0,154 nm. Prawdziwy wzór strukturalny benzenu nie powinien zawierać prostych i podwójnych wiązań. Dlatego węglowodory aromatyczne są klasyfikowane jako nienasycone związki organiczne tylko formalnie. W składzie przypominają alkeny, ale mogą wchodzić w reakcje podstawienia, które są typowe dla końcowych węglowodorów. Aromatyczny rdzeń benzenu ma znaczną odporność na utleniacze. Wszystkie te cechy pozwalają nam uznać pierścień za specjalny rodzaj połączenia - nie podwójny i nie pojedynczy.
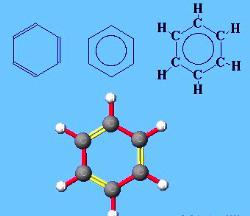
Poprawna jest formuła benzenu nie z trzema podwójnymi wiązaniami, jak w Kekul, ale w postaci sześciokąta z kołem w środku. Symbolizuje wspólną przynależność 6 elektronów.
Potwierdza symetrię struktury iwłasności materii. Pierścień benzenowy jest stabilny, ma znaczną energię koniugacji. Właściwości pierwszego przedstawiciela węglowodorów aromatycznych przejawiają się w jego homologach. Każdy z nich może być przedstawiony jako pochodna, w której wodór zastępuje różne rodniki węglowodorowe.
</ p>